Καλά νέα για τα αγέννητα παιδιά μας!
Τα μωρά με συγγενή καρδιοπάθεια ξεκινούν τη θεραπεία τους ήδη από τη μήτρα!
Εμβρυϊκή Χειρουργική για τα Συγγενή Καρδιακά Νοσήματα.
Δεν υπάρχει ζωικό πειραματικό μοντέλο που να προσομοιάζει ικανοποιητικά ως προς την ανατομία και τη παθοφυσιολογία και να μας βοηθά στις καρδιακές (δε. και αρ.) ανωμαλίες αποφρακτικού τύπου που παρατηρούνται στον άνθρωπο. Ωστόσο, η ανάπτυξη των υπερήχων επέτρεψε την πρωιμότερη και ακριβέστερη διάγνωση των εμβρυϊκών καρδιακών ανωμαλιών, και έδωσε τη δυνατότητα, ιδιαίτερα για το πεδίο των συγγενών καρδιακών νοσημάτων, να γίνει καλύτερα κατανοητή η ιδιαίτερη αιμοδυναμική του εμβρύου και οι μηχανισμοί που εμπλέκονται στην εξέλιξη της καρδιακής νόσου στη μήτρα.
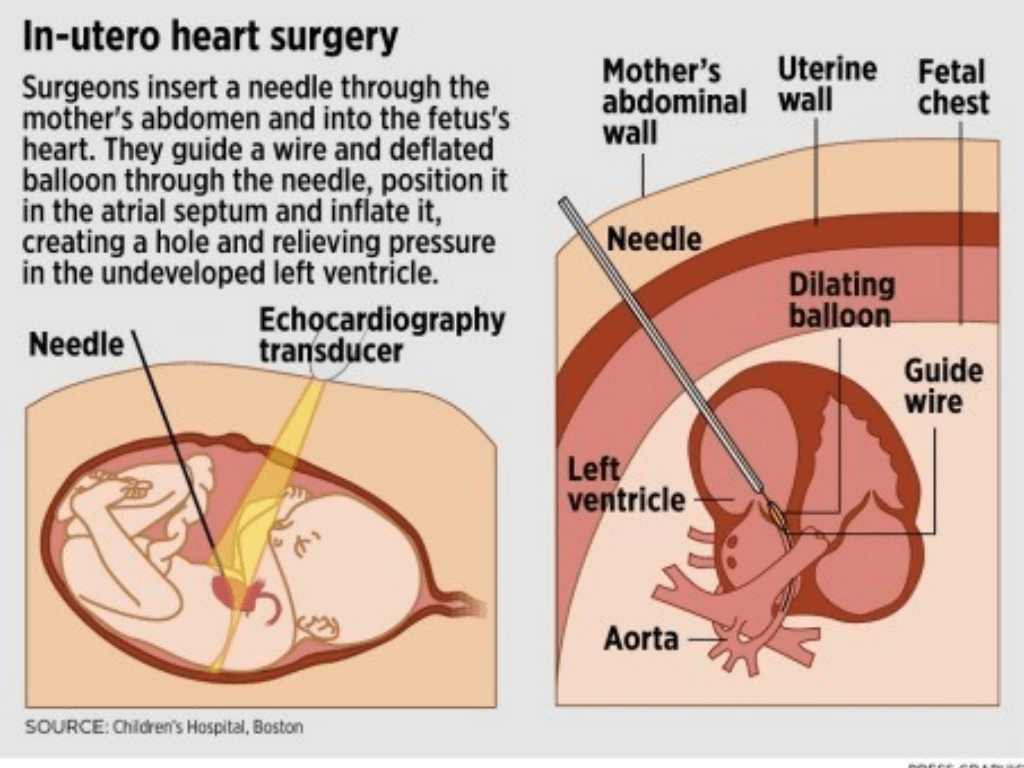
Δεδομένης της σημαντικής πλέον γνώσης, που αφορά την εμβρυϊκή φυσιολογία, τη φυσική ιστορία των καρδιακών ανωμαλιών από τη μήτρα, και μετά την επιτυχία της βαλβιδοπλαστικής με μπαλόνι, που αφορά την αορτική και πνευμονική βαλβίδα, για πρόληψη ή αναστροφή της κοιλιακής δυσλειτουργίας στα νεογέννητα βρέφη, τώρα υπάρχει μια θεωρητική λογική για παρέμβαση με στόχο να βελτιωθεί μια βαλβιδική στένωση, από την εμβρυϊκή ζωή.
Υπάρχει, επίσης, ένα φυσιολογικό και πρακτικό επιχείρημα για τη διεύρυνση της μεσοκολπικής επικοινωνίας στα έμβρυα με περιορισμένο μεσοκολπικό διάφραγμα και αριστερή κολπική υπέρταση, τα οποία διαφορετικά θα παρουσίαζαν συγγενείς ανωμαλίες στα πνευμονικά τους αγγεία και ασταθή αιμοδυναμική λειτουργία εξαιτίας της μικρής ή ανύπαρκτης μεσοκολπικής επικοινωνίας.
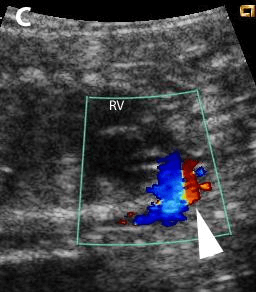
Ο έλεγχος για καρδιακές ανωμαλίες του εμβρύου, περιλαμβάνεται στον προληπτικό έλεγχο της εγκύου και στις οδηγίες εμβρυϊκής παρακολούθησης [1] αποτελεί μάλιστα επέκταση των υπηρεσιών και των πρωτοκόλλων κλινικών ερευνών, που σχετίζονται με την εμβρυϊκή θεραπεία. Θεωρείται σε μεγάλο βαθμό συμπλήρωμα στη βέλτιστη διαχείριση του παιδιού μετά τον τοκετό, χωρίς όμως να αποκλείει την ανάγκη για περαιτέρω καρδιολογική παρέμβαση και αντιμετώπιση μετά τη γέννηση του παιδιού.
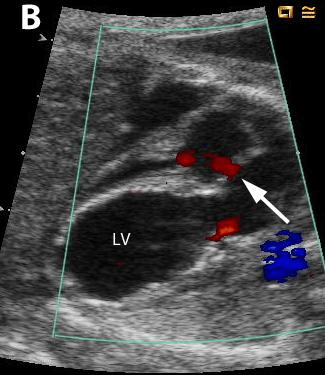
Λόγω βέβαια των πιθανών επιπλοκών, όπως ισχύει για οποιαδήποτε ενδομήτρια παρέμβαση, η επένδυση σε αυτή τη καινοτόμο εμβρυϊκή θεραπεία μπορεί να θεωρηθεί χρήσιμη μόνο όταν η εφαρμογή της είναι εφικτή από απόψεως διαδικαστικής ευκολίας και χαμηλού ποσοστού κινδύνων.
Πειραματικές μελέτες με ανοιχτή καρδιοχειρουργική επέμβαση στο έμβρυο άρχισαν τη δεκαετία του 1980 σε μοντέλα ζώων, ώστε να μελετηθούν στο έμβρυο οι παθοφυσιολογικοί μηχανισμοί της εξωσωματικής κυκλοφοριακής παράκαμψης και οξυγόνωσης. [2] Παρόλο που η αρχική έρευνα έδειξε κάποια αναπαραγωγιμότητα σε αυτή την τεχνική, η εμβρυοπλακουντιακή ανταπόκριση στην εξωσωματική παράκαμψη και οξυγόνωση της κυκλοφορίας του εμβρύου (bypass), είχε ως τελικό αποτέλεσμα την υποξία και τον θάνατο του εμβρύου, κατάληξη που αποθάρρυνε τις ελπίδες πλήρους επιτυχίας.
Οι παράγοντες που συνέβαλλαν στη δυσλειτουργία του πλακούντα, μετά την περίοδο του bypass στην οξυγόνωση, φαίνονταν να είναι πολλαπλοί, με αναφορές για τον τραυματισμό που προκαλείται από ποικίλους εκλυόμενους διαβιβαστές φλεγμονής, και την επαγόμενη δυσλειτουργία στο ενδοθήλιο της καρδιάς και των αγγείων [3, 4, 5, 6]. Ακολούθησε μητρική πλακουντιακή δυσλειτουργία, λόγω της αύξησης των αγγειακών αντιστάσεων, και μια κατάσταση σχετικής υποξίας του εμβρύου, ως συνέπεια της ελαττωμένης αιματικής ροής. [7, 8, 9] Ως αποτέλεσμα, η ανοικτή καρδιοχειρουργική του εμβρύου εγκαταλείφθηκε σε μεγάλο βαθμό.
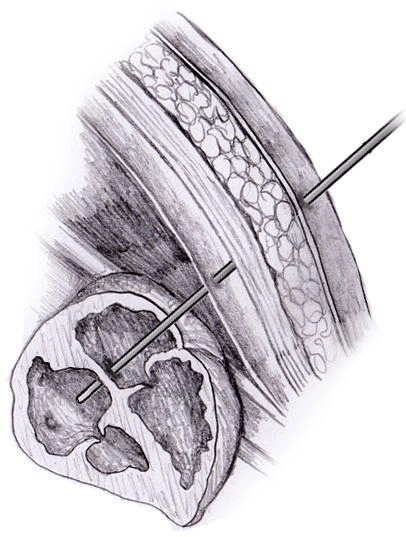
Η παλαιότερη καρδιολογική θεραπεία του ανθρώπινου εμβρύου έγινε το 1975 και αφορούσε τη διαπλακουντιακή χορήγηση, από τη μητέρα στο έμβρυο, ενός β-blocker, για ρύθμιση της κοιλιακής ταχυαρρυθμίας του εμβρύου. [10]
Η πρώτη ανοικτή καρδιολογική in-utero (εντός της μήτρας) επέμβαση, αναφέρθηκε μια δεκαετία αργότερα, το 1986, με τοποθέτηση βηματοδότη σε έμβρυο πάσχον από πλήρη κολποκοιλιακό αποκλεισμό. [11]
Η ιδέα της πραγματοποίησης βαλβιδοπλαστικής με μπαλονάκι, στα έμβρυα με στενωμένες καρδιακές βαλβίδες, ακολούθησε την επιτυχή εισαγωγή της βαλβιδοπλαστικής των νεογνών με μπαλονάκι στη δεκαετία του '80, με την πρώτη αναφερθείσα περίπτωση να εκτελείται σε έμβρυο με αορτική στένωση το 1989. [12]
Η τροποποίηση των πρώιμων αυτών τεχνικών επέτρεψε από τότε τις επεμβάσεις με διαδερμική πρόσβαση και χρήση καθετήρων, και γνώρισε τεχνική επιτυχία όχι μόνο στη στένωση της εμβρυϊκής αορτικής βαλβίδας, αλλά και στην στένωση και ατρησία των βαλβίδων της πνευμονικής αρτηρίας, καθώς και στο σύνδρομο της υποπλαστικής αριστερής καρδιάς (HLHS) με άτρητο ή πολύ περιορισμένα ανοικτό μεσοκολπικό διάφραγμα. [13, 14]
Οι αναφορές για την κλινική πορεία των μωρών, που υπεβλήθησαν σε αυτές τις επεμβάσεις, όπως δίνονται από τις μεγαλύτερες σειρές αυτών των επεμβάσεων, επιβεβαιώνουν την τεχνική τους επιτυχία και την αναπαραγωγιμότητα. [15, 16] Υποδεικνύουν, επίσης, ότι οι επιτυχείς εμβρυϊκές επεμβάσεις οδηγούν σε βελτιωμένη λειτουργική ανάπτυξη των κοιλιών και του μυοκαρδίου, ενώ το έμβρυο παραμένει ακόμη στη μήτρα.
Άλλα επιστημονικά Κέντρα έχουν επίσης αναπαράγει τις αρχικές επιτυχίες [17,18], και τα στοιχεία που αποδεικνύουν ότι η βαλβιδοπλαστική του εμβρύου, που πάσχει από ατρησία ή στένωση των βαλβίδων της αορτής ή της πνευμονικής αρτηρίας, μπορεί να διευκολύνει την ικανότητα διεξαγωγής της κυκλοφορίας και από τις δύο κοιλίες μετά τη γέννηση, ενώ η διαφραγματοπλαστική για τα άτρητα ή με σοβαρό περιορισμό μεσοκολπικά διαφράγματα, μπορεί να βελτιώσει τη μεταγεννητική κυκλοφορική σταθερότητα και τις πιθανότητες επιβίωσης μετά την αρχική ανακουφιστική χειρουργική επέμβαση. [19, 20]
Θεωρείται, επίσης, πιθανό, ότι το ενδομήτριο περιβάλλον είναι εκ φύσεως ευνοϊκό για την επούλωση τραυμάτων και την αναγέννηση σε κυτταρικό επίπεδο. [21] Ωστόσο, πρέπει να καταβάλλεται μεγάλη προσπάθεια για τον κατάλληλο σχεδιασμό των επεμβάσεων και την επιλογή των υποψηφίων (τόσο μητέρων όσο και κυοφορούμενων παιδιών), ώστε να ελαχιστοποιηθούν οι πιθανές επιπλοκές και οι κίνδυνοι που συνδέονται με τις in utero επεμβάσεις.
Ως ενδείξεις για εμβρυϊκή καρδιολογική επέμβαση, θεωρούνται οι ακόλουθες καταστάσεις [22, 23]: Στένωση αορτής , Ατρησία ή περιορισμένη μεσοκολπική επικοινωνία, Πνευμονική ατρησία με ανέπαφο το μεσοκοιλιακό διάφραγμα (PA-IVS), Πλήρης κολποκοιλιακός αποκλεισμός με ύδρωπα.
Τον Μάιο του 2014, η American Heart Association (AHA) εξέδωσε επιστημονική ανακοίνωση σχετικά με τη διάγνωση και τη θεραπεία της καρδιακής νόσου στο έμβρυο [24]. Εκεί αναφέρθηκε ότι η παρέμβαση μέσω καθετήρα στην καρδιά του εμβρύου μπορεί να τεθεί ως θεραπευτική επιλογή στις εξής περιπτώσεις (ιατρική προτροπή κατηγορίας IIb, στοιχεία αποδεδειγμένης αποτελεσματικότητας B / C):
- Στα έμβρυα με στένωση της αορτής, με προωθητική αιματική ροή και εξελισσόμενο Σύνδρομο Υποπλαστικής Αριστερής Καρδίας (HLHS).
- Στα έμβρυα με στένωση της αορτής, σοβαρή παλινδρόμηση στη μιτροειδή και περιορισμένη μεσοκολπική επικοινωνία.
- Στα έμβρυα με Σύνδρομο Υποπλαστικής Αριστερής Καρδίας (HLHS), με σοβαρά περιορισμένο ή άθικτο μεσοκολπικό διάφραγμα.
- Σε έμβρυα με PA-IVS (σύνδρομο που χαρακτηρίζεται από ατρησία της πνευμονικής αρτηρίας και άθικτο μεσοκοιλιακό διάφραγμα).
Σχόλιο «Αφήστε με να Ζήσω!»: Ο άνθρωπος, από τη σύλληψή του, είναι μοναδικός και ανεπανάληπτος. Αξίζει κάθε τιμής και σεβασμού. Οι ασθένειες δεν είναι λόγος για να χαρακτηρίζεται μια ζωή ανεπιθύμητη ή με λιγότερη αξία.
Παρόλα αυτά, όμως, τα ανωτέρω επιστημονικά δεδομένα είναι εξαιρετικά ενθαρρυντικά και στηρίζουν τους γονείς στην απόφαση να κρατήσουν το αγέννητο μωρό τους, που πάσχει από συγγενή καρδιοπάθεια και να το θεραπεύσουν.
Στο εξωτερικό και ευχόμαστε σύντομα και στην Ελλάδα, το μωρό μπορεί να ξεκινήσει την θεραπεία και αποκατάστασή του, ενώ ακόμη βρίσκεται στη μήτρα.
Αναφορές:
- Moon-Grady AJ, Baschat A, Cass D, Choolani M, Copel JA, Crombleholme TM, et al. Fetal Treatment 2017: The Evolution of Fetal Therapy Centers - A Joint Opinion from the International Fetal Medicine and Surgical Society (IFMSS) and the North American Fetal Therapy Network (NAFTNet). Fetal Diagn Ther. 2017 May 23.
- Turley K, Vlahakes GJ, Harrison MR, Messina L, Hanley F, Uhlig PN. Intrauterine cardiothoracic surgery: the fetal lamb model. Ann Thorac Surg. 1982 Oct. 34(4):422-6.
- Sabik JF, Assad RS, Hanley FL. Prostaglandin synthesis inhibition prevents placental dysfunction after fetal cardiac bypass. J Thorac Cardiovasc Surg. 1992 Apr. 103(4):733-41; discussion 741-2.
- Fenton KN, Zinn HE, Heinemann MK, Liddicoat JR, Hanley FL. Long-term survivors of fetal cardiac bypass in lambs. J Thorac Cardiovasc Surg. 1994 Jun. 107(6):1423-7.
- Sabik JF, Heinemann MK, Assad RS, Hanley FL. High-dose steroids prevent placental dysfunction after fetal cardiac bypass. J Thorac Cardiovasc Surg. 1994 Jan. 107(1):116-24; discussion 124-5.
- Reddy VM, McElhinney DB, Rajasinghe HA, Rodriguez JL, Hanley FL. Cytokine Response to Fetal Cardiac Bypass. J Matern Fetal Investig. 1998 Mar. 8(1):46-9.
- Reddy VM, McElhinney DB, Rajasinghe HA, Liddicoat JR, Hendricks-Munoz K, Fineman JR. Role of the endothelium in placental dysfunction after fetal cardiac bypass. J Thorac Cardiovasc Surg. 1999 Feb. 117(2):343-51.
- Parry AJ, Petrossian E, McElhinney DB, Reddy VM, Hanley FL. Neutrophil degranulation and complement activation during fetal cardiac bypass. Ann Thorac Surg. 2000 Aug. 70(2):582-9.
- Reddy VM, Liddicoat JR, Klein JR, McElhinney DB, Wampler RK, Hanley FL. Fetal cardiac bypass using an in-line axial flow pump to minimize extracorporeal surface and avoid priming volume. Ann Thorac Surg. 1996 Aug. 62(2):393-400.
- Eibschitz I, Abinader EG, Klein A, Sharf M. Intrauterine diagnosis and control of fetal ventricular arrhythmia during labor. Am J Obstet Gynecol. 1975 Jul 1. 122(5):597-600.
- Carpenter RJ Jr, Strasburger JF, Garson A Jr, Smith RT, Deter RL, Engelhardt HT Jr. Fetal ventricular pacing for hydrops secondary to complete atrioventricular block. J Am Coll Cardiol. 1986 Dec. 8(6):1434-6.
- Maxwell D, Allan L, Tynan MJ. Balloon dilatation of the aortic valve in the fetus: a report of two cases. Br Heart J. 1991 May. 65(5):256-8.
- Kunisaki SM, Jennings RW,Fetal Surgery. J Intensiv Care Med, 2008, 23: 33-51.
- Cortes RA, Farmer DL. Recent advances in fetal surgery. Semin Perinatol. 2004 Jun. 28(3):199-211.
- Tworetzky W, Wilkins-Haug L, Jennings RW, van der Velde ME, Marshall AC, Marx GR. Balloon dilation of severe aortic stenosis in the fetus: potential for prevention of hypoplastic left heart syndrome: candidate selection, technique, and results of successful intervention. Circulation. 2004 Oct 12. 110(15):2125-31.
- Moon-Grady AJ, Morris SA, Belfort M, et al. for the International Fetal Cardiac Intervention Registry. International Fetal Cardiac Intervention Registry: A Worldwide Collaborative Description and Preliminary Outcomes. J Am Coll Cardiol. 2015 Jul 28. 66 (4):388-99.
- Tworetzky W, McElhinney DB, Marx GR, Benson CB, Brusseau R, Morash D. In utero valvuloplasty for pulmonary atresia with hypoplastic right ventricle: techniques and outcomes. Pediatrics. 2009 Sep. 124(3):e510-8.
- Arzt W, Wertaschnigg D, Veit I, Klement F, Gitter R, Tulzer G. Intrauterine aortic valvuloplasty in fetuses with critical aortic stenosis: experience and results of 24 procedures. Ultrasound Obstet Gynecol. 2011 Jun. 37(6):689-95.
- Rychik J, Rome JJ, Collins MH, DeCampli WM, Spray TL. The hypoplastic left heart syndrome with intact atrial septum: atrial morphology, pulmonary vascular histopathology and outcome. J Am Coll Cardiol. 1999 Aug. 34(2):554-60.
- Marshall AC, Levine J, Morash D, et al. Results of in utero atrial septoplasty in fetuses with hypoplastic left heart syndrome. Prenat Diagn. 2008 Nov. 28(11):1023-8.
- Gurtner GC, Werner S, Barrandon Y, Longaker MT. Wound repair and regeneration. Nature. 2008 May 15. 453(7193):314-21.
- Freud LR, Tworetzky W. Fetal interventions for congenital heart disease. Curr Opin Pediatr. 2016 Apr. 28 (2):156-62.
- Gellis L, Tworetzky W. The boundaries of fetal cardiac intervention: Expand or tighten? Semin Fetal Neonatal Med. 2017 Dec. 22 (6):399-403.
- Donofrio MT, Moon-Grady AJ, Hornberger LK, Copel JA, Sklansky MS, Abuhamad A, et al. Diagnosis and treatment of fetal cardiac disease: a scientific statement from the American Heart Association. Circulation. 2014 May 27. 129(21):2183-242.
Πηγή: https://emedicine.medscape.com/article/2109511-overview#a3